股市瞬息万变,投资难以决策?来#A股参谋部#超话聊一聊,[点击进入超话]
财熵|资本离场,君实生物的新冠药物故事不灵了?
原创 吴楠 财熵
导读:近些年来,君实生物可谓流年不利:2018年摘得首个国产PD-1桂冠,却在2019年错失了医保先机;2020年以降价7成的代价换取入保资格,却陷入销售收入负增长的尴尬境地;如今就连“新冠特效药”这个新故事,似乎也不灵了。
作者|吴楠
主编|谷越
版式|九五
2020年初,新冠肺炎疫情席卷全球。作为防疫的重要手段,新冠疫苗与新冠特效药被外界寄予厚望,亦成为不少药企竞逐的对象。
新冠疫苗方面,经过第一轮的竞速筛选,目前已经进入第二轮“加强针”竞赛。可以窥见的是,当初火爆的疫苗市场,如今已有供过于求之势。
反观新冠特效药赛场,国内药企研发仍如火如荼,不少企业全力冲刺,希望能够抢先撞线。
作为新冠特效药赛道上的领跑选手,君实生物(688180.SH,01877.HK)于今年5月23日宣布,其新冠口服药VV116与辉瑞的Paxlovid头对头III期临床试验,达到主要终点,同时表明已递交新药上市申请。
药物研发取得突破性进展本是喜事一桩,但事情的走向却有些出人意料:官宣次日,君实生物在港股大跌近13%,在A股科创板更是暴跌20%,以跌停价收盘,令广大投资者愕然。
或许可以用“流年不利”一词来形容君实生物近几年的境遇——2018年摘得首个国产PD-1桂冠,却在2019年错失了医保先机;2020年以降价7成的代价换取入保资格,却陷入销售收入负增长的尴尬局面;如今就连新冠特效药这个新故事,似乎也不灵了。除此之外,这些年君实还遭遇了商业化推广不力、销售高管动荡、PD-1出海受阻等诸多坎坷。
成立10年,从未盈利,君实生物该拿什么来换取资本市场的信任?
PD-1“起了个大早,赶了个晚集”
2018年12月,君实生物打败恒瑞医药(600276.SH)、百济神州(688235.SH)等老牌药企,成功拿下首个国产PD-1桂冠,在国内创新药江湖一战成名。(注:PD-1,在临床上称之为PD-1抑制剂,属于一种免疫抑制分子,是治疗肿瘤的新型药物)
在此之前,君实生物名不见经传,从未有产品面世,以至于自2012年成立以来,业绩连年亏损。就是这样一家籍籍无名的小企业,凭什么能够成为中国PD-1先锋?
有人将其归功于君实生物的灵魂人物、创始人陈博——科研出身的他,一手主导了PD-1的立项、研发。
也有人认为,君实生物的成功离不开掌门人熊俊及其父熊凤祥。尽管二人的“非生物医学背景”曾备受外界质疑,但不可否认,金融出身的熊俊确实为君实出了不少力。
要知道,创新药是一项十分烧钱的生意,在医药界向来有“双十定律”之说——一款创新药从研发到上市,平均需要十年研发周期,十亿美元投入。
在PD-1产品问世之前,君实生物主要依靠转让技术许可等方式获取收入。但这与其动辄数以亿计的研发费用相比,显得不值一提。既然造血能力不足,那就只能依靠外界输血。
在熊俊的资本运作下,君实生物于2015年8月在新三板挂牌上市,并在短短两年多的时间里先后进行了7次定增融资,合计募集资金超过18亿元人民币(如无特殊注明,货币单位下同);随后,公司又于2018年12月登陆港交所,IPO募集金额为30.8亿港元;2020年7月登陆A股科创板,IPO募集48.36亿元。
值得一提的是,高瓴资本也曾在2016年、2018年向君实生物递去过橄榄枝。
2018年12月,君实生物的特瑞普利单抗注射液“拓益”首发上市,引发医药界与投资界轰动。作为当时市面上最热门的“抗癌神药”,PD-1有着非常广阔的前景。据弗若斯特沙利文预测,2030年全球PD-1/PD-L1药物的市场规模将达到789亿美元,国内市场可达988亿元。
率先撞线的君实生物,理所当然被寄予厚望,投资者期盼着PD-1能够带领君实扭转多年来持续亏损的局面。
然而,越是有利可图的赛道,无疑越是拥挤。早在君实生物获批上市之前,2018年6月、7月,跨国药企百时美施贵宝(BMY.NYSE)的Opdivo和默沙东(MRK.NYSE)的Keytruda就先后以“全球最低价”进入中国;2018年12月-2019年12月,信达生物(01801.HK)的达伯舒、恒瑞医药的艾立妥、百济神州的百泽安相继获批上市,君实生物的先发优势几乎消失殆尽。
2019年底,君实生物在医保谈判中遗憾落选,反倒是信达生物后来居上,成为“首个且唯一”纳入国家医保目录的PD-1药企。有人评价道,在PD-1赛道上,君实“起了个大早,赶了个晚集”。这句话在此后几年里,仍以不同的形式伴随其左右。
2020年,凭借医保优势,信达生物PD-1产品实现销售额24.9亿元。同期百济神州实现11.2亿的销售额,恒瑞医药虽未入医保,却拥有强大的销售队伍和成熟的销售渠道,当年其PD-1销售额高达约45亿元,而君实生物则以约10亿元的销售额在四大国产PD-1企业中垫底。
这其中的差距显而易见。截至2020年底,君实生物的销售团队为912人,相比2019年的360人翻了一倍多;而同期信达生物、百济神州的销售团队均超过千人,恒瑞医药的销售团队更是高达17000多人。
强敌环伺,君实生物选择了破釜沉舟。2020年底,君实PD-1不惜以降价7成的代价纳入医保。2021年2月,君实又宣布与阿斯利康制药(AZN.NASDAQ)达成商业化合作,授予其特瑞普利单抗在中国大陆地区后续获批上市的泌尿肿瘤领域适应症的独家推广权,以及所有获批适应症在非核心城市区域的独家推广权,协议期限为5年。
原本想“以价换量”,却未料遭现实狠狠浇了一盆冷水——2021年全年,君实生物的PD-1单抗销售收入仅为4.12亿元,相较于2020年的10.03亿元,销售额同比下降约60%。
这背后,诚然有进入医保目录后价格大幅降低的原因,也有君实生物在适应症方面的劣势因素:2020年医保谈判时,君实PD-1获批的适应症只有黑色素瘤一项,国内患者相对较少;更关键的,还是源于君实在商业化能力上过于拉胯。
除了在销售人员上的不足之外,另外一个可以佐证的事实是,2021年至今,君实生物已有多位负责PD-1商业化的高管相继离职,与之合作的阿斯利康在中国的县域销售团队同样动荡不安,以至于双方牵手不到一年时间,即2022年1月4日,君实便宣布与阿斯利康终止PD-1单抗的推广合作。
君实生物在2021年年报中坦承:“2021年亦是公司商业化团队较为动荡的一年,公司团队先后经历了几轮商业化负责人及内部营销人员的调整,并与外部合作方就特瑞普利单抗的推广合作进行共同探索和磨合。频繁的团队更迭导致队伍稳定性受到很大影响,团队执行力下降,市场活动不能稳定执行,市场活动有效性下降,客户合作信心受到很大影响。”
如今,君实生物在PD-1赛道上严重掉队已是不争的事实,未来能否在创新药市场扭转乾坤,新冠特效药或是关键。
新冠药物领跑反遭资本市场重锤
与早期的PD-1一样,君实生物在新冠特效药赛道上,也是名副其实的领跑选手。
早在2020年3月20日,君实生物就宣布开始研发新冠病毒抗体药品,代号为JS016;不到3个月时间,JS016便获批进入I期临床试验阶段。这是全球首个进入临床阶段的新冠病毒中和抗体品种,甚至领先于再生元(REGN.NASDAQ)、安进(AMGN.NASDAQ)等诸多跨国知名药企。
效率如此之高,主要得益于中科院微生物所和国家传染病医学中心主任张文宏的相助。前者在新冠疫情爆发初期利用自身的平台筛选出抗体序列,随即将JS016抗体的商业开发权授予君实生物,后者则主导了该药物的临床试验。
需要指出的是,在进入临床试验之前,即2020年5月,君实生物就将JS016在中国之外的研发、生产和销售的独占许可授予了美国企业礼来制药(LLY.NYSE)。作为回报,礼来向君实支付了1000万美元首付款,并承诺在实现规定的里程碑事件后支付最高2.45亿美元的里程碑款,外加该产品销售净额两位数百分比的销售分成。
随着2021年JS016在全球超过15个国家和地区获得紧急使用授权并成功实现销售,当年君实生物从礼来制药处获得技术许可及特许权收入约为23.66亿元,占公司当年总营收50%以上。
除了JS016之外,君实生物在研管线还有另外3款新冠治疗药物,分别为JS026、VV116和VV993。
JS026属于中和抗体药物,目前尚处在临床试验阶段;VV116和VV993为口服药物,均由中国科学院上海药物研究所、武汉病毒研究所等共同研发,并由君实生物的控股子公司君拓生物与旺山旺水负责合作开发和商业化。VV993属于3CL蛋白酶抑制剂,研发时间较短,目前还处于临床前研究阶段。
VV116属于口服核苷类抗新冠病毒药物,2021年底已在乌兹别克斯坦获批紧急使用授权,用于中重度COVID-19患者的治疗;在国内,今年5月23日,君实生物宣布该款药物已达到临床方案预设的主要终点,这意味着距离其获批上市指日可待。
然而,VV116的“超速”进展并没有给君实生物带来预期中的利好,反而令其在资本市场惨遭重锤——5月24日-6月1日,君实生物股价在A股、港股分别跌超31%、25%。
之所以会有如此“异常”的表现,一方面源于业内对VV116的安全性、临床试验数据等信息存疑。对此,君实生物曾回应称,VV116总体安全性良好,总体不良事件发生率低于PAXLOVID;另一方面,则因为市场对VV116未来的商业化能力抱有分歧,毕竟有PD-1这一前车之鉴摆在眼前。
严格来说,VV116是目前国产小分子新冠口服药中研发进度最快的品种之一,距离上市只剩“临门一脚”。但其先发优势并不算特别突出,开拓药业(09939.HK)的普克鲁胺也处于临床三期,而真实生物的阿兹夫定早在今年4月时就已结束了三期临床,只不过获批上市还迟迟未能落定。
财熵注意到,国家药品监督管理局药品评审中心的沟通交流公示显示,今年以来君实生物共提交了10次沟通交流会议申请,其中6月的两项II类会议,目前处于“处理中”状态;而真实生物总共申请过2次会议,最新的一次III类会议停留在4月2日,处于“已反馈”状态。II类会议中就包含了“新药上市许可申请前会议”,看样子,君实生物对于争夺“首个国产新冠口服药”的名号是势在必得。
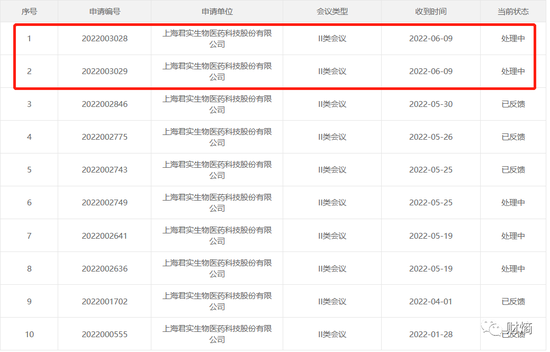
君实生物积极提交沟通交流会议申请图源药监局审评中心
故事还未讲完,机构已开始离场
6月1日,外资投行麦格理发布了一篇看空报告,授予君实生物“跑输大市”评级,造成当日公司A股、港股股价双双暴跌。麦格里在报告中提到,预计VV116将于第三季取得紧急使用授权,虽然对获批持乐观态度,但预计产品的商业应用仍存在不确定性,包括要面对市场竞争、需求未明及定价问题等。
麦格理的担忧不无道理,要知道,在新冠特效药赛道上,君实生物从不缺对手。
目前,国内已经获批了两款新冠特效药:腾盛博药(02137.HK)的BRII-198/BRII-198和美国辉瑞(PFE.NYSE)的Paxlovid。
BRII-198/BRII-198为中和抗体类药物,是我国自主研发的首款抗新冠病毒药物,已于2021年12月8日在中国获批上市;而君实生物的JS016虽然早已实现销售,但战场主要在海外,且公司靠的是专利费和销售分成盈利,收入可谓大打折扣,即便如今转战国内,也已然失了先发优势。
Paxlovid于2021年12月22日通过美国FDA紧急使用申请,2022年2月11日在国内获批附条件上市,属于口服小分子药物,与君实生物的VV116形成正面对抗。
目前国内新冠特效药研发管线主要包括口服小分子药物、单克隆抗体、3CL 蛋白酶性质特效药、核苷类药物等,几乎每一条赛道上都有诸多玩家。据财熵不完全统计,国内布局新冠口服药物的企业就已超过10家。
即便是君实生物得以从众多竞争对手中突围,拔得国产新冠口服药头筹,未来或也将面临带量采购、销售不佳等风险,又或者遭受如新冠检测价格一降再降的境遇。
“按照集采规则,一般需要符合申报条件的企业数≥3家,或者说有一定的议价空间,才会去组织相关的集采动作。”诚存资本创始合伙人、广东省药品交易中心三医药械电子交易管理有限公司执行总裁方贤赟向财熵表示,“与当初的PD-1一样,未来随着新冠药物研发的不断推进,可能会提出相应的集采行为,但主要还是得看供需关系有没有得到充分的满足。”
目前国内疫情形势已整体趋于平稳,而海外市场对新冠药物却表现出强烈的需求——再生元/罗氏的Ronapreve于2020年11月获FDA紧急使用授权,2021年即实现销售额75.74亿美元;默沙东的莫努匹韦(Molnupiravir)上市仅一个多月,便实现了9.52亿美元的销售收入。
在此背景下,出海,或将成为君实生物等新冠特效药企业的出路之一。
不过,能否成功出海还存在较大的不确定性,毕竟此前君实生物的核心产品特瑞普利单抗就已闯关FDA失败。当然,这些都得等到VV116上市之后再做筹谋。而今君实显然有着更为棘手的问题需要应对。
根据财报显示,2021年君实生物实现营业收入40.25亿元,扣非净利润却为-8.84亿元。公司在年报中坦承:“由于营业收入尚不能覆盖不断增长的研发费用及其他开支,公司2021年度尚未实现盈利。”
财熵梳理发现,2021年全年,君实生物的研发费用高达20.69亿元,另外“三费”合计14亿元。而今年一季度,公司“研发+三费”为8.45亿元,甚至高于同期6.3亿元的营收。(注:三费,即销售、管理、财务)
需要指出的是,截至今年一季度末,君实生物的账上仅躺着42.6亿货币现金,若公司的商业化产品无法持续贡献收入,且在研产品获批进展不顺,那么按其2021年的投入力度,公司已经没有多少钱可以烧了。
为了及时补血,早在今年3月7日,君实生物便抛出一份拟募资不超过39.8亿元的定增方案。这份方案曾引来上交所问询,后经调整,于6月15日重新公布,募集资金下调为不超过39.69亿元,其中36.71亿元用于创新药研发项目,2.98亿元用于科技总部及研发基地项目。
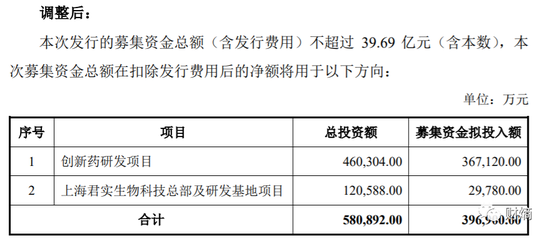
君实生物定增方案 图源公司公告
君实生物的定增方案还未真正落地,但资本离场潮已经开始上演——2021年三季度,高瓴资本从A股君实生物的十大股东中退出,同期离场的还有易方达基金、社保基金等多家机构投资者。如今君实的前十大流通股东中,有一半以上为个人投资者。
君实生物已成立十年,回顾过往,它并没有很好地把握住PD-1带来的机遇,如今新冠特效药江湖格局未定,它还能讲好这一故事吗?

责任编辑:梁斌 SF055


 产品入口: 新浪财经APP-股票-免费问股
产品入口: 新浪财经APP-股票-免费问股


 产品入口: 新浪财经APP-股票-免费问股
产品入口: 新浪财经APP-股票-免费问股
 产品入口: 新浪财经APP-股票-免费问股
产品入口: 新浪财经APP-股票-免费问股
APP专享直播
热门推荐
收起
24小时滚动播报最新的财经资讯和视频,更多粉丝福利扫描二维码关注(sinafinance)









