转自:医药观澜
7月14日,中国国家药监局药品审评中心(CDE)官网最新公示,渤健(Biogen)递交了5.1类新药托夫生注射液的上市申请,并获得受理。公开资料显示,这是渤健和Ionis Pharmaceuticals联合开发的反义寡核苷酸(ASO)疗法Qalsody(tofersen),也是FDA批准治疗遗传性肌萎缩侧索硬化(ALS)的首款疗法。
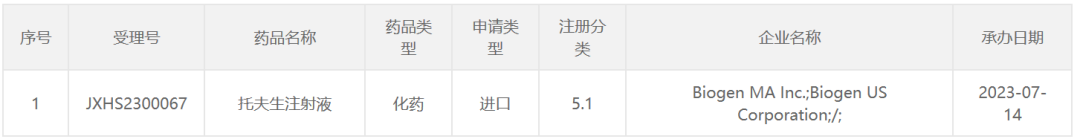 截图来源:CDE官网
截图来源:CDE官网肌萎缩侧索硬化症(ALS)是一种进行性神经退行性疾病,影响大脑和脊髓中的神经细胞,也被称为“渐冻症”。这种疾病的患者大脑和脊柱的运动神经元会不断死亡,导致患者的肌肉无力和瘫痪,从无法行走到无法说话、吞咽、呼吸。ALS患者在确诊后平均寿命小于5年。目前,许多基因被认为与此疾病有关联,其中具有超氧化物歧化酶1(SOD1)突变的患者(SOD1-ALS)约占了2%。这些患者中大部分疾病进展迅速,发病后甚至无法活过1年。
Tofersen是一种在研反义寡核苷酸药物,正在开发用于治疗SOD1-ALS。该药可以与编码SOD1的mRNA结合,造成其被核糖核酸酶RNase-H降解,进而减少突变的SOD1蛋白生成。

为期6个月的3期临床试验结果显示,其试验并未达成其主要终点——患者根据ALS功能评分量表修订版(ALSFRS-R),自基线至试验28周评分的变化差异。然而生物标志物研究显示,该药可显著降低患者体内SOD1蛋白水平,且降低了与神经轴突损伤相关的神经丝轻链(NfL)的水平。此前,美国FDA外周和中枢神经系统药物咨询委员会以9:0的投票结果,支持基于生物标志物变化加速批准tofersen治疗SOD1-ALS患者。
今年4月,FDA宣布加速批准tofersen上市,用于治疗具有SOD1突变的肌萎缩侧索硬化。这一批准不但为具有SOD1突变的ALS患者带来了具有针对性的疗法,对基于生物标志物加速神经退行性疾病的疗法开发也具有重要意义。
为了证实tofersen的临床益处,一项3期随机、双盲、安慰剂对照试验正在对尚未出现症状的SOD1基因突变携带者进行。这项研究将评估与安慰剂相比,接受该产品治疗的ALS患者在试验期间出现ALS症状的比例。
参考资料:
[1]中国国家药监局药品审评中心(CDE)官网. Retrieved July 14, 2023, from https://www.cde.org.cn/main/xxgk/listpage/9f9c74c73e0f8f56a8bfbc646055026d
[2] FDA approves treatment of amyotrophic lateral sclerosis associated with a mutation in the SOD1 gene. Retrieved April 25, 2023, from https://www.fda.gov/drugs/news-events-human-drugs/fda-approves-treatment-amyotrophic-lateral-sclerosis-associated-mutation-sod1-gene
[3]Ionis accounces FDA advisory committee voted unanimously for a potential accelerated approval of tofersen for SOD1-ALS . Retrieved Mar 22,2023, from https://ir.ionispharma.com/news-releases/news-release-details/ionis-accounces-fda-advisory-committee-voted-unanimously#:~:text=Ionis%20accounces%20FDA%20advisory%20committee%20voted%20unanimously%20for,ALS%20and%20the%20next%20marketed%20Ionis-discovered%20antisense%20medicine

VIP课程推荐
APP专享直播
热门推荐
收起
24小时滚动播报最新的财经资讯和视频,更多粉丝福利扫描二维码关注(sinafinance)











