来源:“十点科学”微信公众号
病毒变异给全球防疫不断带来一轮轮新的挑战。变强之后的病毒,到底哪里不一样了?

德尔塔变异株已在全球132个国家蔓延|news.cgtn.com
撰文/徐斯佳 ([日]京都大学医学院)
最近,新冠病毒德尔塔(Delta)变异株在国内的跨省传播引发高度关注。其实该病毒在全球范围内已经传播很长时间了。
德尔塔变异株病毒载量高、传播能力强、传播速度快,转阴时间长。自2020 年10 月首次在印度出现以来,11个月的时间内已扩散至全球132个国家地区,导致多国新冠病例激增,对未接种疫苗人群的健康和全球经济复苏产生严重影响。(联合国7月30日数据)
世界卫生组织流行病学家Maria van Kerkhove指出,德尔塔变异株的传染力比2019年底首次出现的原始毒株高出约50%。
德尔塔变异株为何传染性这么强?现有的疫苗还能保护我们吗?
新冠病毒是怎么变异的
生物的亲代和子代之间总有些差异,这是群体多样性和进化发展所必须的。病毒虽然是自己复制自己,在此过程中基因也会发生频繁的突变,产生变异株。这种突变原本是随机的,效果也不确定。有些可能不会令病毒产生明显变化;有些反而会使病毒变得更温和;自然,也有一些会令病毒的传播力、毒性都更强。
所谓“适者生存”。如果某些变异能让病毒更容易感染宿主,或逃避免疫系统的攻击,就有更多机会大量复制,产生同样狡猾或强势的子代。然后像滚雪球一样,队伍不断壮大,对公共卫生造成新的威胁。
其实这种现象在病毒世界里普遍存在。一个典型例子就是艾滋病病毒HIV。正是因为HIV极高的突变率,令疫苗和治疗药的研发非常艰难。精心设计的作用靶点(即反应位置)很容易因病毒变异而失去预期效果。
再说回新冠病毒。我们知道,它们感染人体细胞的关键就是其表面的刺突蛋白(Spike Protein), 一般有24~40个,呈任意排列。它们像一把把“钥匙”,锚定细胞上的“锁”(受体分子)进入人体细胞,大肆复制、造成伤害。刺突蛋白也是疫苗研发的重点目标。
刺突蛋白的底部有像关节一样的“铰链”结构,又能令其灵活摆动、旋转,增加蛋白与细胞接触的机会;而蛋白顶端有多个与细胞结合的关键部位:受体结合域(RBD)。危险的变异株多在这里发生重要突变。
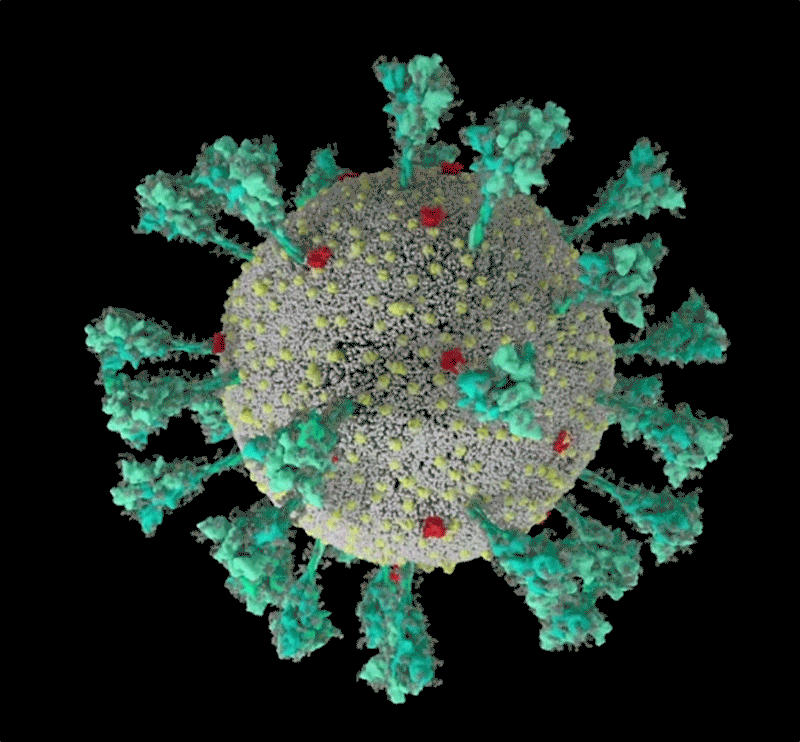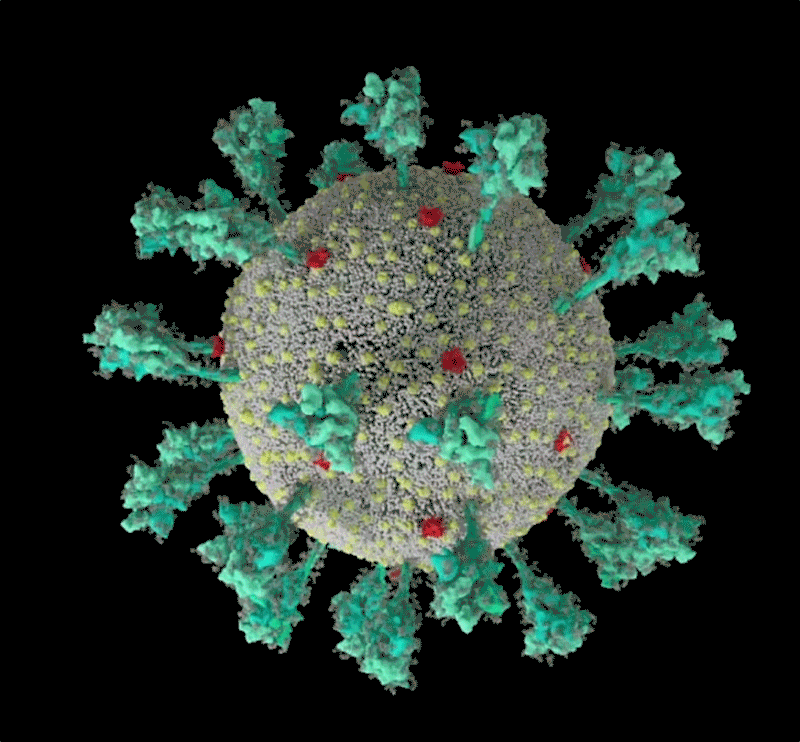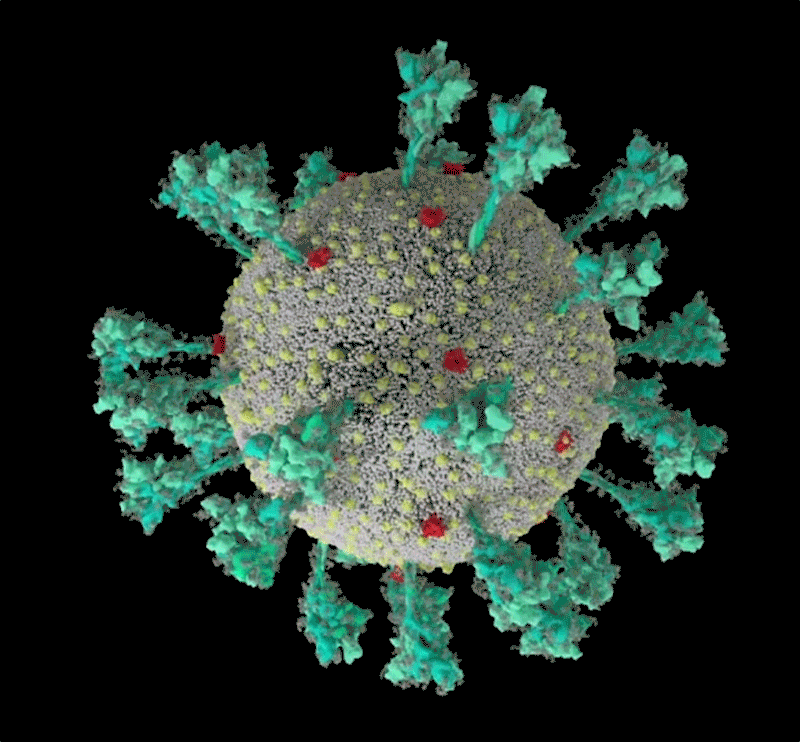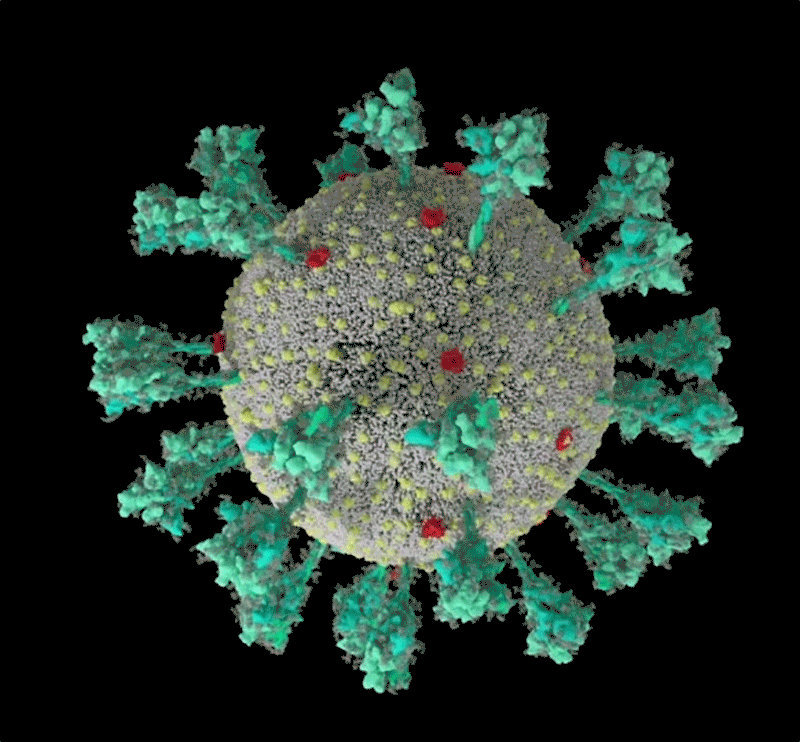
新冠病毒的计算机模拟结构, 绿色即为刺突蛋白。可以看出其形态非常多变,这让它与人体细胞结合的方式也更加多样。| University of Utah
“传染王”德尔塔有何特别之处
根据危险程度不同,世卫组织将新冠变异毒株分成两类:令人担忧的变异株(VOC, variant of concern)和值得关注的变异株(VOI, variant of interest)。前者是指引发的病例多、范围广,并已有数据证实其传播能力、毒性强,或导致疫苗和临床治疗有效性降低;后者则是虽在世界范围内出现社区传播病例,但尚未形成大规模传染。
显而易见,VOC对公共健康威胁较大,是需要重点应对的类型。其中包括:在英国占主导的阿尔法变异株(Alpha)、南非的贝塔(Beta)、巴西的伽马(Gamma)和在印度率先发现的德尔塔(Delta)。按希腊字母命名的做法,是为了避免对变异株发现的国家造成污名化。
刺突蛋白顶部受体结合域的突变可能直接影响病毒入侵细胞的能力。有的突变能导致 RBD保持“向上”状态不易坍塌,从而更容易进入细胞。德尔塔变异株的受体结合域上有 3 个突变,与细胞的亲和力更强。作为比较,阿尔法变异株的传播率比新冠病毒原始毒株高 50%,而德尔塔比阿尔法变种又高出约 60%。
不过,要做到传染性强,容易进入细胞还不够,病毒还得抢夺宿主细胞大量自我复制,以及具备逃避免疫系统打击的本领。
人体的细胞工厂原本不是为了复制病毒服务的,每时每刻都在忙着自己的蛋白质合成。新冠病毒抵达细胞内部后首先合成一种病毒蛋白(Nsp1),它会切割不带病毒标记的人体细胞的核酸(携带着基因信息),令需要完整信息才能产生的人体蛋白无法合成。
病毒把细胞工厂大肆占为己有,同时关闭细胞的预警系统。正常情况下,当细胞察觉到自己被感染,一部分特殊的基因会被激活,合成出能预警人体免疫系统的物质(如干扰素),释放出去召唤救兵。而又是Nsp1蛋白,它能阻塞细胞核的通道,不让那些核酸接触细胞工厂,也就无法合成预警蛋白,更遑论向外呼救,免疫系统便很难注意到被感染细胞发出的求救指令。

狡猾的新冠病毒,不仅阻碍细胞正常蛋白质合成,还不让“报警”|维基百科
德尔塔病毒变异株不仅继承了所有这些诡计,成为“传染王”的它还另有一绝招。
新冠病毒的刺突蛋白上下各亚基之间有个特殊的位点,称为“弗林(Furin)切割位点”,因为它能被宿主细胞的弗林蛋白识别并切割。切割后,病毒颗粒的刺突蛋白会松开,暴露出里面和细胞膜性质相同的疏水性区域,将自己迅速与宿主细胞膜融为一体。普通冠状病毒也有这个位点,但一般只有一个精氨酸。新冠病毒的此处却是个由 5 个氨基酸(脯氨酸、精氨酸、精氨酸、丙氨酸、精氨酸)连成的“链子”,更容易被识别。

Furin蛋白酶的切割使刺突蛋白结构变得松散,因而能够被一种名为TMPRSS2的蛋白酶识别并被继续切割,从而暴露出其中的疏水氨基酸,进而得以快速进入细胞。图为TMPRSS2蛋白酶切割刺突蛋白。|Nature
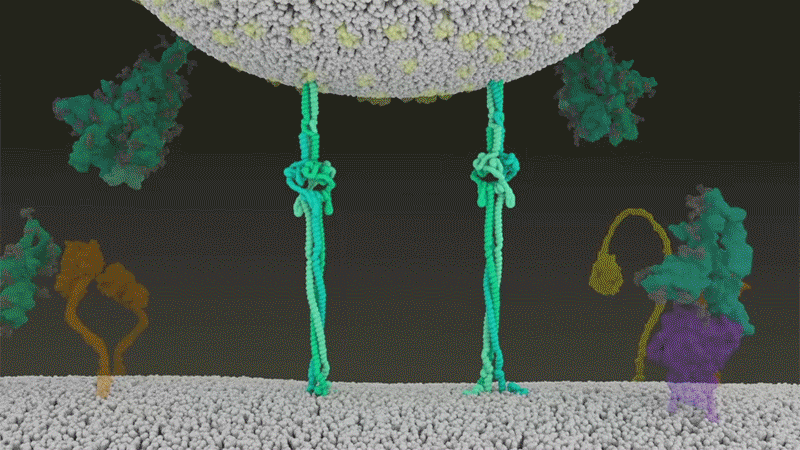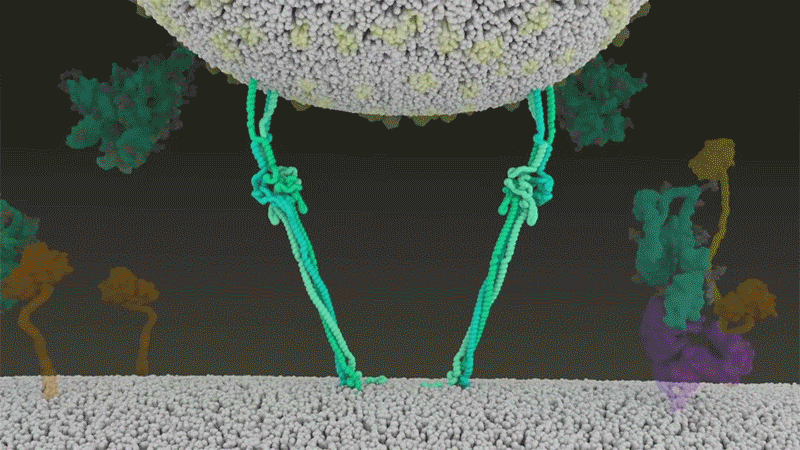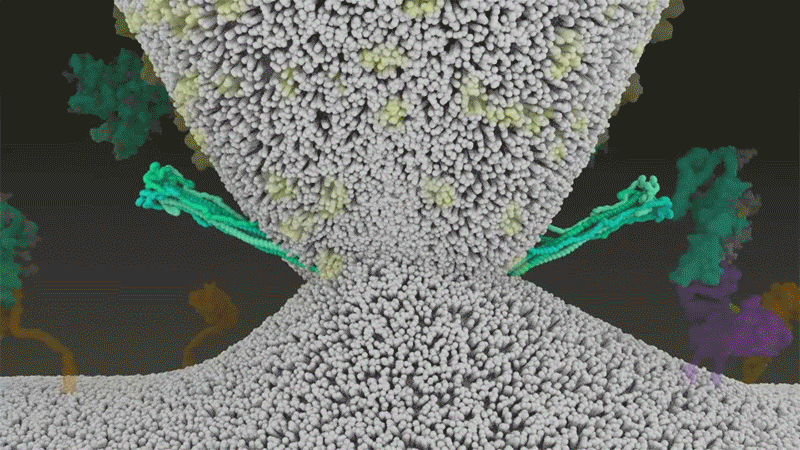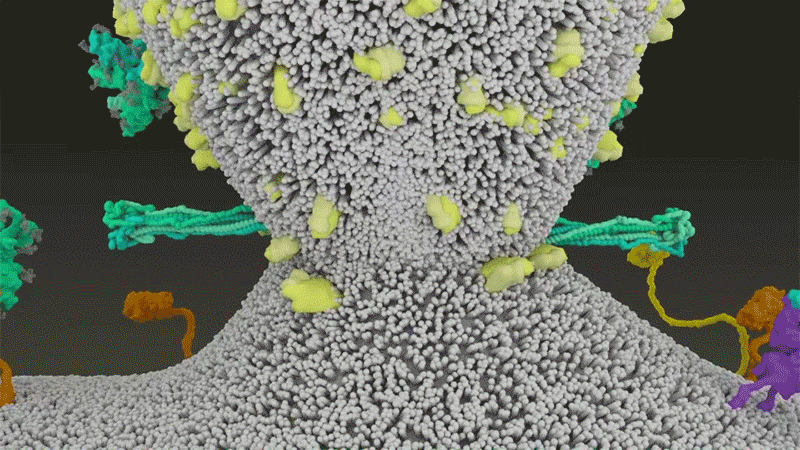
刺突蛋白附着在细胞膜上之后,通过折叠自身,拉扯病毒与细胞膜融合。|Nature
阿尔法和德尔塔变异株的弗林切割位点都发生了变化。前者将原来的脯氨酸替换成组氨酸;而德尔塔则替换成了精氨酸。这两个变化都会减少这条“链子”的酸性。氨基酸链的碱性越高,切割的效果越好。更多切割意味着更多刺突蛋白准备好进入人体细胞。SARS病毒只有不到 10% 的刺突蛋白做好了这种准备,阿尔法毒株超过了50%,而德尔塔变异株这一比例高达75% 以上,成为其超强传染能力的重要原因。
所幸,传染性更高并不意味着更致命。目前数据表明德尔塔变异株虽然更容易攻击50岁以下的较年轻的人群,使多地住院率上升。但并没有证据支持其更致命。
完善疫苗接种有助于抵抗变异株
眼下主流的疫苗如灭活疫苗、核酸疫苗,基础免疫程序均为2剂次。各国正在对疫苗混搭、加打第三剂的方案展开研究,找出防范德尔塔变异株的有效策略。
7月初,德国卫生部下属的常务疫苗委员会(STIKO)提议:已接种了第一针阿斯利康腺病毒载体疫苗的人群,第二针施打BioNTech/辉瑞或者莫德纳的核酸疫苗可获得 “极佳”的保护力,且间隔期可从12周缩短至最少4周,“这对于防范德尔塔变种蔓延有着重大意义”。
我国也在积极开展第三针加强针的效果研究。
7月25日,科兴疫苗发布了一项研究结果(同行评审中)。该研究从2020年5月开始展开,共540名受试者参与。受试者被分为4组,先以14天和28天为间隔接种2剂科兴灭活疫苗,再以28天和180天接种第3剂疫苗。
结果发现第三针可大幅提升人体免疫反应,中和抗体滴度较接种两针后提高数倍。但针对变异株是否有相同效果仍待研究。

各国都在研究新的疫苗接种方案。|图虫创意
紧随其后,美国辉瑞/BioNTech也公布了核酸疫苗BNT162b2的加强针数据,对于德尔塔变异株,成年组接种第三针后,抗体滴度由241升至1321,提高超过4倍;老年组中,抗体滴度从124上升至1479,提高超过10倍。
虽然接种第三针可使中和抗体滴度明显提高,但目前相关方案还没正式推广。
当然,中和抗体数量并不是衡量疫苗好坏的唯一指标,人体免疫系统也并非对被感染的细胞束手无策。
美国克利夫兰诊所的一项样本量超过5.2万的研究发现:曾感染过新冠病毒的人,5个月内抵抗再次感染的能力与注射疫苗相当。对于未感染过的人们来说,完成疫苗注射,不仅能获得可靠的防护,也有助于减少病毒的携带与传播等(包括无症状感染者)。
钟南山院士曾提醒,我国需要83.3%的接种率才能达到群体免疫,特别呼吁重视疫苗接种。
这是一场时间的竞赛。在疫情大肆复燃,或更棘手的变异出现之前,应尽可能争取让更多人接种疫苗。其他话不多说,保持距离、戴好口罩。
(注:刚刚,一项新的研究指出,目前正在南美地区快速传播的拉姆达变异株,与原始版本相比,具有高度传染性,对疫苗的耐药性也更强。有分析认为,按照目前的传播趋势,拉姆达有可能取代德尔塔,成为下一阶段全球流行的优势毒株。)
(责编 高佩雯)
参考资料
1.https://www.medrxiv.org/content/10.1101/2021.06.17.21259103v1
2.https://www.thelancet.com/journals/lancet/article/PIIS0140-6736(21)01358-1/fulltext
3。Hoffmann M, Kleine-Weber H, Pöhlmann S。 AMultibasic Cleavage Site in the Spike Protein of SARS-CoV-2 Is Essential forInfection of Human Lung Cells。 Mol Cell。 2020 May 21;78(4):779-784.e5。 doi:10.1016/j.molcel.2020.04.022。 Epub 2020 May 1。 PMID: 32362314; PMCID: PMC7194065。

“掌”握科技鲜闻 (微信搜索techsina或扫描左侧二维码关注)