无风不起浪,李连达院士与A股公司天士力复方丹参滴丸的“纠葛”再次激起了世人对中药的讨论:既有人对“药现代化和国际化”表示认可;也有人对“用西医方法检验中医中药”提出疑问。但不管双方怎样博弈,其讨论基调均是对中药有着高度的认可。
“韭菜”们清一色地认可中药,但在李连达院士的公开“吹牛在前,失败在后,始于谎言,毁于欺骗”的指责下,二级市场的主力还是借“言”洗盘,让天士力股价应声跌落了不少。
截至9月18日收盘,智通财经观察到,该股跌4.21%,报价35.74元人民币,市值一日之内便蒸发了16.95亿人民币,损失颇为惨重。

行情来源:富途证券
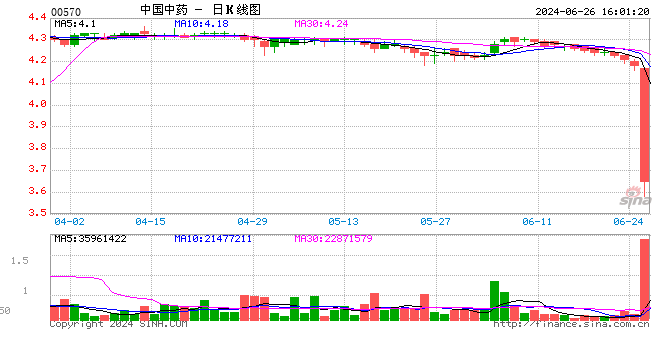
天士力的复方丹参滴丸“风波”,虽未对港股医疗保健形成正面冲击,可在该板块成分股中,雅各臣(02633)、同仁堂科技(01666)、中国中药(00570)等多只中药股呈现微跌状态。不难让人联想到或与复方丹参滴丸“风波”有关。毕竟“同根生,相煎急”。

行情来源:富途证券
复方丹参滴丸“风波”不断
时间回到8月31日,天士力公告了与FDA就复方丹参滴丸(T89)新药申报可行性议题会议的结论,讨论了T89治疗慢性稳定性心绞痛作用机理及国际多中心Ⅲ期临床研究T89-07-CAESA试验的结果,以及T89的巨大市场需求和临床价值,并与FDA共同探讨了早日审批T89上市的可行性。

本来是利好一件,奈何近日,曾任职于天士力的李连达院士,却在科学网个人博客上针对天士力公司产品复方丹参滴丸美国FDAⅢ期临床试验公开发表了《丹参滴丸三期临床惨遭失败,损失惨重,教训惨痛》的文章。内容直指天士力明星产品复方丹参滴丸是国际药物申请史上的骗局。
智通财经留意原文中,“天士力公司在中国境内宣传“复方丹参滴丸”通过美国FDA”申请,而真正在美国申请的药是‘丹通尼克胶囊’。滴丸和胶囊是不同剂型的药,从药学上看‘丹通尼克胶囊’和‘复方丹参滴丸’是二种不同的药。制造工艺完全不同,CGMP的要求完全不同,制药中最核心的CMC文件完全不一样。”
此外,该文质疑,通过美国FDA II期临床试验的复方中药制剂并不能就证明是安全和有效的,这与天士力方面的宣传并没有因果的逻辑关系。
我发利好,你质疑。天士力赶紧在9月15日发布澄清声明称,该文章编造吸引眼球的虚假标题,内容与事实严重不符,这些违法的、错误的言论,可能对投资者和消费者造成误导。

声明中,天士力还特意披露了公司与李连达院士的关系,原来十多年前双方就接下“梁子”。同时,该公司表示对李连达的违法行为,保留追究其法律责任的权利。

其实,这并非复方丹参滴丸首次被质疑。2016年12月9日,全欧中医药联合会副主席祝国光发表《天士力公司在美国临床试验上的骗局》等博文,直指天士力在向美国FDA申报并开展临床研究的药物并非其宣传的复方丹参滴丸。祝国光认为,天士力此举是利用信息不对称等,通过不断虚假宣传做大销售,并在股市上大肆圈钱。
同样,在事件发酵几天后,天士力发布澄清公告称,发现科学网祝国光个人博客多次出现不实言论,恶意攻击天士力和复方丹参滴丸产品,经出具法律文件,科学网及时删除了不实文章。澄清公告中也披露了企业和祝的关系,“祝曾担任过天士力多年的技术顾问,但合同到期终止后,还多次索要不当费用,却未达到目的,其言论歪曲事实,用所谓的专业性误导投资者。”
对于当时的澄清,祝国光也是直接回复:“正义只是晚到,从来不会缺席。这是造假者惯用手法,现在天士力已经承认在美国做的是胶囊剂,而不是复方丹参滴丸。”
同样的“澄清”文,同样的套路,加上目前FDA官方文件未公布,智通财经财经APP也法判断究竟是谁在说谎?不过,随着时间推移,真相肯定只有一个。
临床试验复杂至极
上述两位质疑都提到了天士力复方丹参滴丸的临床试验“造假”问题,既然聊到临床,智通财经不妨先给大伙普及下什么叫临床试验:
第一步,动物实验。研发人员提炼出某个分子后,会进行动物试验(小白鼠什么的),主要是看这个分子对其细胞、机能有什么反应,以达到评估效果和安全性的目的,比如药理、毒理、代谢等,特别涉及安全性证据。
第二步,人体临床试验。先向CFDA、FDA提交材料申请,通过审评后,再根据批准文件联系医院,做临床性试验。因为涉及到人,还得通过伦理委员会的批准。像经常有媒体爆料的“试药人群”,其实就是在做人体临床试验。

第三步,临床试验约三期。一期主要是评估副作用、代谢特征等等,一般选十来个样本;二期验证适应症的安全权,会选100个样本以上;三期继续验证药物的有效性和安全性,采取双盲对照,会搞300甚至万个的样本做试药,这期是最花钱的,失败风险也是较大的,而这些费用、失败风险一般都是企业承担。
第四步,安全通过申请上市。企业会和CFDA、FDA去商讨报批上市的条件,并递交申请。别以为走到这步就是成功了,因为药监局也会检查中间的临床试验步骤,评审该药物是否符合“绿色通道”,假如临床试验步骤有问题,也是拿不到上市批文的(比如2015年爆发的银杏叶引发的临床数据清查事件)。
第五步,上市后的继续做4四期临床试验(目的是大范围进一步验证药物的安全性和有效性)以及上市再评价工作。
按照这一复杂流程,天士力的复方丹参滴丸在三期临床阶段,是最花钱、也是风险较大的阶段。但因为复方丹参滴丸属于中医,所以在临床阶段更加复杂,况且FDA也没有一套“标准”的现代化中药的评审标准。因此,天士力屡遭质疑也情有可原。
中药做临床是大趋势
事实上,中药做临床的提议已经提及多年,虽然2016年下发的《中医药法(草案)》中表示,凡“符合条件的、来源于古代经典名方的中药复方制剂,在申请药品批准文号时,可以仅提供非临床安全性研究资料。”
之所以不做“临床”,支持派表示,“经典药方”是经过长期使用,其安全性、有效性早已确认,而且日本、韩国的经方也没有进行临床试验。可这样的理由显然在面对 “安全、稳定性”等问题是不充分的。
智通财经分析发现,我国中药成方制剂经过近30年快速发展共计拥有9000多个品种,大约80%存在基础研究薄弱、临床适应证宽泛的问题,个别药品甚至包治百病,使西医临床和患者对中药产生不信任感,存在认知误区,在一定程度上阻碍了中药的发展。
举个简单例子,中药说明书适应证模糊,不适应现代医学病症的情况较为普遍,这导致了西医不敢用中药,不会用中药,不愿用中药,也给用药安全造成了隐患,比如中药现代化的创新中药注射剂。
2012年全国药品不良反应监测网共收到14个大类中药注射剂报告10.3万例次,其中严重报告5500余例次,占比为5.3%。据国家药品不良反应监测中心2013年的统计,在收到的药品不良反应病例报告中,中药不良反应事件病例报告仅占总数的17.3%,但中药注射剂的不良反应事件病例却占中药病例报告的70%以上;2015年全国药品不良反应监测网络共收到中药注射剂报告12.7万例次,注射剂占比例为51.3%。
现状之下,国家从2009年开始开展中药注射剂的临床安全性再评价和按病种分类的改革。而中国中药协会制定的《中药协会药物临床评价研究专业委员会管理办法》、《中药协会药物临床评价研究专业委员会评价学组工作细则》以及《中药协会药物临床评价研究专业委员会科研课题管理办法》等多个临床评价文件。
从这点不难推出,中药未来肯定是要做临床的。因为只有拿出具有说服力的研究数据,国际才会认可,才能抢占全球市场。所以,在港股的你,不妨多关注中国中药、同仁堂科技等中药股的药物创新,毕竟中医药这一民族精粹是不会死的。(田宇轩/文)
进入【新浪财经股吧】讨论
责任编辑:张海营